INTRODUCTION TO THE INSTITUTE

可生物降解的級(jí)聯(lián)納米催化劑用于腫瘤微環(huán)境重構(gòu),實(shí)現(xiàn)可控的CO釋放和腫瘤靶向/協(xié)同治療
文章標(biāo)題:Biodegradable cascade nanocatalysts enable tumor-microenvironment
remodeling for controllable CO release and targeted/synergistic cancer nanotherapy
第一作者:Jianrong Wu
通訊作者:Xiaojun Cai,Yu Chen, and Yuanyi Zheng
通訊單位:上海交通大學(xué)附屬第六人民醫(yī)院,上海大學(xué)
論文導(dǎo)讀:
氣體療法作為一種新興的腫瘤治療方式,由于其低的毒副作用,具有廣闊應(yīng)用前景的治療策略。然而這種治療模式仍面臨著諸多挑戰(zhàn),如治療性氣體的精確遞送和可控釋放。針對(duì)這一挑戰(zhàn),上海交通大學(xué)附屬第六人民醫(yī)院鄭元義教授、蔡曉軍副研究員和上海大學(xué)陳雨教授等合作報(bào)道了一種級(jí)聯(lián)生物可降解納米催化劑介導(dǎo)的原位持續(xù)釋放CO氣體和磁共振成像監(jiān)測(cè)的靶向/協(xié)同腫瘤氣體/饑餓納米治療的“腫瘤微環(huán)境重塑”策略。該納米催化劑通過(guò)將葡萄糖氧化酶(GOD)和H2O2敏感分子羰基錳(MnCO)包裹在可生物降解的中空介孔有機(jī)硅納米粒子中制備而成。GOD首先作為介孔氧化硅的“開(kāi)關(guān)”,隨后修飾靶向多肽(cRGD)用于特異性靶向αvβ3整合素過(guò)表達(dá)的腫瘤細(xì)胞。在腫瘤微酸性的情況下,GOD被解離,釋放負(fù)載的MnCO前藥。前藥在H2O2的條件下原位釋放CO氣體。同時(shí),GOD催化腫瘤細(xì)胞內(nèi)葡萄糖分解產(chǎn)生葡萄糖酸和H2O2來(lái)重塑腫瘤微環(huán)境,進(jìn)一步促進(jìn)CO/Mn2+的原位生成。通過(guò)細(xì)胞實(shí)驗(yàn)和體內(nèi)異位腫瘤模型驗(yàn)證表明:納米催化劑通過(guò)協(xié)同CO氣體和饑餓納米治療,可以獲得了優(yōu)越的治療性能。本研究為通過(guò)重塑腫瘤微環(huán)境增強(qiáng)CO介導(dǎo)的抗腫瘤療效提供了一種新的策略。
研究進(jìn)展:
在這項(xiàng)工作中,研究人員設(shè)計(jì)了一種智能的靶向/級(jí)聯(lián)納米催化劑(RGD-GOD-MnCO@HMONs,縮寫為RG-Mn@H) 重構(gòu)TME,實(shí)現(xiàn)CO氣體的原位可控釋放。構(gòu)建的級(jí)聯(lián)納米催化劑可在磁共振(MR)引導(dǎo)下用于協(xié)同腫瘤饑餓治療與CO氣體治療(圖一)。在TME中,通過(guò)GSH誘導(dǎo)的二硫鍵斷裂和pH誘導(dǎo)的亞胺鍵水解打開(kāi)GOD門衛(wèi),繼而使得HMONs的快速生物降解,導(dǎo)致負(fù)載MnCO的釋放,MnCO進(jìn)一步與內(nèi)源性H2O2和H+反應(yīng)以實(shí)現(xiàn)CO氣體的按需釋放。隨后,釋放的GOD催化葡萄糖生成葡萄糖酸和H2O2。這一過(guò)程不僅切斷了細(xì)胞的營(yíng)養(yǎng)來(lái)源,而且通過(guò)H+和H2O2富集的TME的重構(gòu),加速了MnCO的分解,提高了CO的生成。同時(shí),基于釋放出的順磁性Mn2+離子,磁共振T1加權(quán)成像也可以監(jiān)測(cè)治療過(guò)程。該方法在體外和體內(nèi)都得到了系統(tǒng)的評(píng)價(jià)和驗(yàn)證。
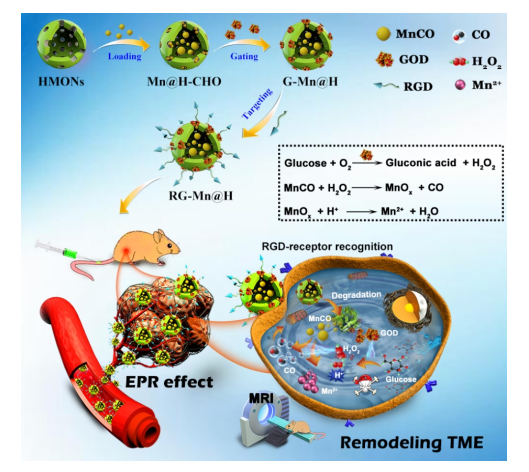
圖一 靶向級(jí)聯(lián)納米催化劑(RG-Mn@H)的設(shè)計(jì)及其用于TME的重構(gòu),引發(fā)連續(xù)級(jí)聯(lián)反應(yīng)的示意圖
首先,該團(tuán)隊(duì)采用“氨水輔助選擇性蝕刻”方法合成具有二硫鍵摻雜/結(jié)合的HMON框架。通常,核/殼SiO2@MONs在三乙醇胺存在下制備。用氨水溶液選擇性地刻蝕SiO2核,形成空心納米結(jié)構(gòu)。透射電子顯微鏡(TEM)圖像顯示,獲得的HMON具有均勻的空心球形拓?fù)浣Y(jié)構(gòu),粒徑約為55 nm(圖二a)。相應(yīng)的能譜分析顯示了C、S、Si和O元素的分布。基于29Si魔角自旋(MAS)和13C交叉極化MAS(CPMAS)固態(tài)NMR譜的HMONs組成分析證實(shí)HMONs中存在二硫鍵雜化的倍半硅氧烷骨架(圖二b和c),當(dāng)MnCO封裝后,HMONs-CHO的Zeta電位變?yōu)?16.2 mV(圖二d)。從Mn@H-CHO的紫外-可見(jiàn)光譜可以看出(圖二e),在340 nm處發(fā)現(xiàn)MnCO的顯著吸收,證實(shí)了有效的MnCO封裝,其負(fù)載效率為37.5%(w/w%)。GOD作為門控開(kāi)放,通過(guò)形成pH敏感的亞胺共價(jià)鍵與HMONs-CHO結(jié)合,從而得到一種新的納米催化劑,GOD-MnCO@HMONs (G-Mn@H). 同時(shí),進(jìn)一步修飾RGD形成最終產(chǎn)物RG-Mn@H 納米催化劑。TEM圖像(圖二f)顯示了RG-Mn@H獨(dú)特的球形結(jié)構(gòu),且平均直徑為66.8 nm,略大于原始的HMONs。元素映射圖像也反映了RG-Mn@H 中Si、C、S、O、N和Mn元素的均勻分布(圖二g)。HMONs-CHO的BET比表面積和孔徑在經(jīng)過(guò)藥物加載、隨后的GOD修飾和RGD連接后表現(xiàn)出明顯的減小。逐步改變的Zeta電位進(jìn)一步證明了RG-Mn@H的成功合成(圖二d)。
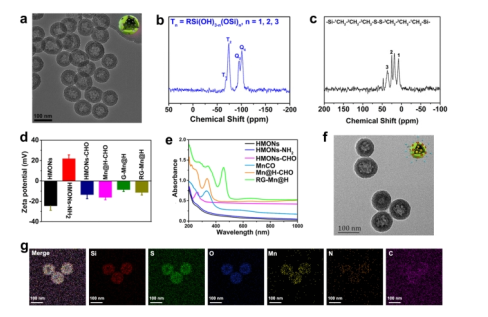
圖二 RG-Mn@H 納米催化劑的表征。(a)HMONs納米粒子的TEM圖像。(b)HMONs的29Si和(c)13C譜。(d)HMONs,HMONs-NH2,HMONs-CHO的zeta電位和(e)紫外-可見(jiàn)吸收光譜。RG-Mn@H的(f)TEM圖像和(g)硅、硫、氧、錳、碳、氮的元素映射mapping圖。
進(jìn)一步評(píng)估RG-Mn@H對(duì)TME的重構(gòu)能力及體外療效。為了深入了解其細(xì)胞內(nèi)吞行為,選擇αvβ3過(guò)表達(dá)的腫瘤細(xì)胞系MDA-MB-231來(lái)評(píng)估納米催化劑的細(xì)胞攝取效率。從激光共聚焦掃描顯微鏡(CLSM)圖像中,RG-Mn@H 與G-Mn@H 組觀察到異硫氰酸熒光素(FITC)熒光信號(hào)的增加(圖三a)。另外,當(dāng)用游離RGD預(yù)處理后再與細(xì)胞孵育時(shí),熒光強(qiáng)度相應(yīng)地降低,證明了RG-Mn@H的靶向性主要?dú)w因于表面連接的RGD與αvβ3整合素蛋白的特異性識(shí)別。流式細(xì)胞術(shù)定量進(jìn)一步證實(shí),通過(guò)RGD修飾,這些納米顆粒的細(xì)胞內(nèi)化顯著增加(圖三b)。結(jié)果證明:納米催化劑良好的細(xì)胞內(nèi)吞作用有助于腫瘤靶向的MnCO轉(zhuǎn)運(yùn)。接著檢測(cè)不同處理后MDA-MB-231細(xì)胞內(nèi)H2O2水平(圖三c)。與PBS和G-Mn@H 治療組相比,RG-Mn@H 處理后的細(xì)胞內(nèi)的H2O2隨著時(shí)間的延長(zhǎng)迅速增加。RG-Mn@H組處理后的細(xì)胞內(nèi)H2O2水平(1.14 mM)比GOD組(0.82 mM)高出約1.5倍。接下來(lái),進(jìn)一步應(yīng)用經(jīng)典的CO熒光探針(COP-1)來(lái)評(píng)估細(xì)胞內(nèi)H2O2驅(qū)動(dòng)的CO釋放。CLSM圖像顯示,R-Mn@H組未檢測(cè)到明顯的綠色熒光,而RG-Mn@H組在pH 5.0下,細(xì)胞內(nèi)的熒光強(qiáng)度隨培養(yǎng)時(shí)間的延長(zhǎng)而顯著增強(qiáng),表明細(xì)胞內(nèi)CO的可控釋放(圖三d)。RG-Mn@H在pH 7.4條件下處理的腫瘤細(xì)胞只有微弱的熒光信號(hào),這可歸因于穩(wěn)定的納米催化劑和中性pH條件下GOD出于關(guān)狀態(tài)。因此,通過(guò)重構(gòu)TME實(shí)現(xiàn)H2O2的自供給來(lái)控制CO的釋放速率和釋放量是可行的。然后我們進(jìn)一步檢查RG-Mn@H的體外治療效果(圖三e)。在沒(méi)有葡萄糖的環(huán)境下,不同納米材料培養(yǎng)的MDA-MB-231癌細(xì)胞的存活率與對(duì)照組接近。相對(duì)而言,通過(guò)RG-Mn@H與葡萄糖進(jìn)行治療,細(xì)胞死亡率顯著(86.8%)。這一結(jié)果表明,葡萄糖是達(dá)到預(yù)期治療效果所必需的。同時(shí)發(fā)現(xiàn)RGD修飾的納米催化劑可以增強(qiáng)對(duì)癌細(xì)胞的細(xì)胞毒性,這是由于主動(dòng)靶向效應(yīng)αvβ3-RGD的特定識(shí)別。同時(shí),細(xì)胞毒性與RG-Mn@H的濃度以及pH值密切相關(guān)。此外,鈣黃綠素-AM/PI染色試驗(yàn)進(jìn)一步驗(yàn)證治療效果(圖三f)。
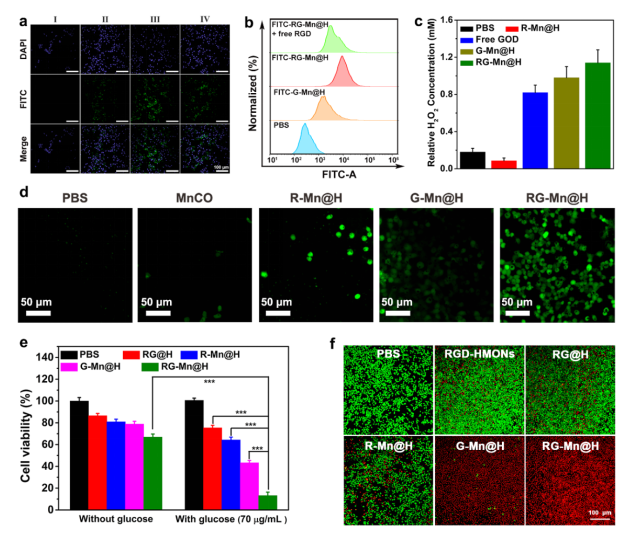
圖 三 (a)不同處理后MDA-MB-231細(xì)胞的共焦熒光圖像。所有比例尺都是50 μm。Ⅰ: PBS;Ⅱ: FITC-G-Mn@H (20 μg/mL);Ⅲ: FITC-RG-Mn@H (20 μg/mL);Ⅳ: FITC-RG-Mn@H (20 μg/mL)+ 游離RGD;(b)不同處理后MDA-MB-231細(xì)胞的流式細(xì)胞術(shù)分析;(b, c)不同處理后MDA-MB-231細(xì)胞內(nèi)H2O2含量的變化。(d)用COP-1型CO熒光探針檢測(cè)細(xì)胞內(nèi)CO含量([Mn]:10μg/mL)。(e)不同處理后MDA-MB-231細(xì)胞相對(duì)存活率([Mn]:10 μg/mL)(f)不同處理后鈣黃綠素-AM和PI共染細(xì)胞的共聚焦圖像。
最后,研究人員對(duì)采用MDA-MB-231乳腺癌模型進(jìn)行評(píng)價(jià)RG-Mn@H的腫瘤治療效果。小鼠隨機(jī)分為五組:PBS組,RG@H,R-Mn@H,G-Mn@H,和RG-Mn@H。 在整個(gè)治療期間監(jiān)測(cè)腫瘤體積和體重。如圖四a所示,采用RG@H治療對(duì)腫瘤生長(zhǎng)無(wú)明顯抑制作用(抑制率為28.6%)。而單獨(dú)使用R-Mn@H的小鼠也僅僅得到一定的靜置(抑制率35.5%)。相比之下,G-Mn@H 治療抑制效果更為顯著(抑制率66.7%)。最顯著的應(yīng)該是協(xié)同納米治療組(RG-Mn@H),其在治療期間有顯著的抑瘤作用(抑瘤率94.3%)。通過(guò)測(cè)定各組代表性小鼠的腫瘤重量和相應(yīng)的數(shù)碼照片進(jìn)一步證實(shí)RG-Mn@H獲得了佳治療效果(圖四b)。與此同時(shí),不同治療組的小鼠體重沒(méi)有明顯變化(圖四c),表明所有制劑引起的副作用可以忽略不計(jì)。值得注意的是,在注射后30分鐘,小鼠的血糖水平略有下降,然后自發(fā)恢復(fù)正常,而在后續(xù)治療過(guò)程中觀察到血糖水平?jīng)]有明顯變化(圖四d)。這一結(jié)果進(jìn)一步表明RG-Mn@H不會(huì)引發(fā)潛在毒性。值得注意的是,RG-Mn@H治療組的小鼠存活率明顯長(zhǎng)于其他治療組(圖四e),進(jìn)一步證明了高協(xié)同抗癌作用。為了揭示其抗腫瘤作用的生物學(xué)機(jī)制,采用蘇木精和伊紅(H&E)、TdT介導(dǎo)的dUTP生物素缺口標(biāo)記(TUNEL)和Ki-67抗體對(duì)各種治療后的腫瘤切片進(jìn)行染色(圖四f)。可見(jiàn),RG-Mn@H處理的老鼠組,在H&E染色圖像上顯示最明顯的凋亡/壞死區(qū),而TUNEL染色顯示腫瘤細(xì)胞凋亡水平最高。同樣地,Ki-67染色顯示腫瘤細(xì)胞的增殖抑制最明顯。
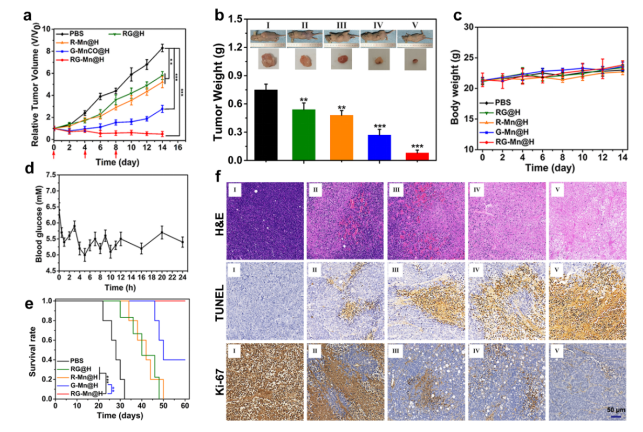
圖四 RG-Mn@H 納米催化劑的體內(nèi)抗腫瘤效果。(a)不同治療模式在治療期間的腫瘤生長(zhǎng)曲線( n= 5)。(b)治療后第14天小鼠腫瘤重量。**P < 0.01,***P < 0.001。插圖:MDA-MB-231荷瘤小鼠的代表性照片和不同治療后小鼠切除腫瘤的相應(yīng)圖像。Ⅰ:PBS;Ⅱ:RG@H; Ⅲ:R-Mn@H;Ⅳ:G-Mn@H;Ⅴ:RG-Mn@H。(c)治療期間小鼠體重變化(n = 5)。(d) 小鼠靜脈注射RG-Mn@H后的血糖水平(n = 5)。(e)不同治療組后MDA-MB-231荷瘤小鼠2個(gè)月生存曲線(n = 5)。(f)MDA-MB-231 荷瘤裸鼠經(jīng)過(guò)不同的治療手段后腫瘤部位的 H&E、TUNEL和Ki67染色圖。比例尺:50 μm。
總結(jié)與展望:
上海交通大學(xué)附屬第六人民醫(yī)院上海超聲醫(yī)學(xué)研究所(超聲醫(yī)學(xué)科)聯(lián)合上海大學(xué)報(bào)告了一種靶向/級(jí)聯(lián)納米催化劑實(shí)現(xiàn)原位可控CO釋放和有效氣體治療的“TME重構(gòu)”。作為一個(gè)范例,類似芬頓的前藥MnCO和天然GOD被同時(shí)整合到可生物降解的HMONs中來(lái)構(gòu)建RG-Mn@H納米催化劑。RG-Mn@H能夠特異性響應(yīng)TME并隨后重構(gòu)TME。當(dāng)被腫瘤細(xì)胞內(nèi)吞時(shí),RG-Mn@H 發(fā)生快速的生物降解同時(shí)打開(kāi)GOD門控開(kāi)關(guān)。隨后,GOD引起的內(nèi)源性葡萄糖消耗的級(jí)聯(lián)反應(yīng)不僅對(duì)腫瘤細(xì)胞的饑餓治療有顯著的作用,而且還通過(guò)提高H2O2水平來(lái)重構(gòu)TME。RGD修飾的納米催化劑具有良好的生物相容性、固有的腫瘤特異性生物降解性和協(xié)同抗癌作用,為αvβ3整合素高表達(dá)的惡性腫瘤的靶向、高效氣體治療提供了一種新的思路。同時(shí)作為智能納米平臺(tái)的例子,RG-Mn@H具有重構(gòu)TME以增強(qiáng)納米治療效果的特定能力。
論文信息:
Biodegradable cascade nanocatalysts enable tumor-microenvironment remodeling for controllable CO release and targeted/synergistic cancer nanotherapy
JianrongWu,ZheyingMeng,AgataA.Exner,XiaojunCai,XueXie,BingHu,YuChen,YuanyiZheng,
Biomaterials
DOI:10.1016/j.biomaterials.2021.121001
原文鏈接:
https://www.sciencedirect.com/science/article/pii/S0142961221003574